伟德源自英国始于19462013届毕业生王燕峰以并列一作在Nature发表文章
转自清华新闻网1月24日电 1月22日,《自然》期刊在线发表了清华大学肖百龙与李雪明课题组合作撰写的《Piezo1离子通道的结构与机械门控机制》(Structure and Mechanogating Mechanism of the Piezo1 Channel)研究论文。论文解析了哺乳动物机械门控Piezo1离子通道的高分辨率三维结构,揭示了其参与机械力感受与传递的关键功能位点,进而首次提出了Piezo通道以类似杠杆原理进行机械门控的精巧工作机制。该研究对理解生物机体如何将机械力刺激转化为电化学信号这一基本生命过程具有重要意义。
机械门控阳离子通道是一类能够响应机械力刺激而引起阳离子进出细胞、进而诱发细胞兴奋和信号传递的一类重要离子通道,但在哺乳动物的分子组成中长期未被发现确定。直到2010年,Piezo基因家族包括Piezo1和Piezo2两个基因被编码为该类通道的必要组成成分 (Coste et al., Science 2010)。2012年,肖百龙博士与同事合作在《自然》期刊报道Piezo蛋白构成机械门控通道的孔道组成成分,从而首次确立了Piezo通道这一全新机械门控离子通道家族。该论文被汤森路透收录为高被引论文。
Piezo通道作为机械力受体能够被挤压、牵张及被流体剪切力等不同形式的机械力所激活。表达在血管内皮细胞中的Piezo1被证实作为剪切力受体感知血流,从而控制血管发育及进行血压调节。而表达在感觉神经细胞中的Piezo2被证实承担触碰及本体感知分子受体的功能。Piezo1基因人类遗传突变,会引发干瘪红细胞增多症、淋巴管发育不良症;而Piezo2基因突变,则会导致远端关节弯曲综合症及触碰感知缺陷。因此,Piezo通道具有非常重要的生理、病理功能,也是重要的药物靶点。
肖百龙博士课题组长期致力于对Piezo通道进行深入系统研究,取得了一系列重要的研究成果。2015年,肖百龙课题组合作在《自然》期刊率先报道了Piezo1通道中等分辨率冷冻电镜三维结构,揭示了其三叶螺旋桨状三维构造特征;2016年,在神经科学重要期刊《神经元》(Neuron) 报道了Piezo1通道负责离子通透与选择性的孔道区模块,以及负责机械力感受与传导的机械传感模块;2017年,在《自然-通讯》期刊报道Piezo通道的新型调控蛋白心肌肌浆网Ca2+-ATP酶(SERCA),并阐明了其对Piezo通道活性调控的作用机制。然而,Piezo通道的高分辨率三维结构及其如何感知机械力并精准控制阳离子特异性通透的分子机制尚不清楚。
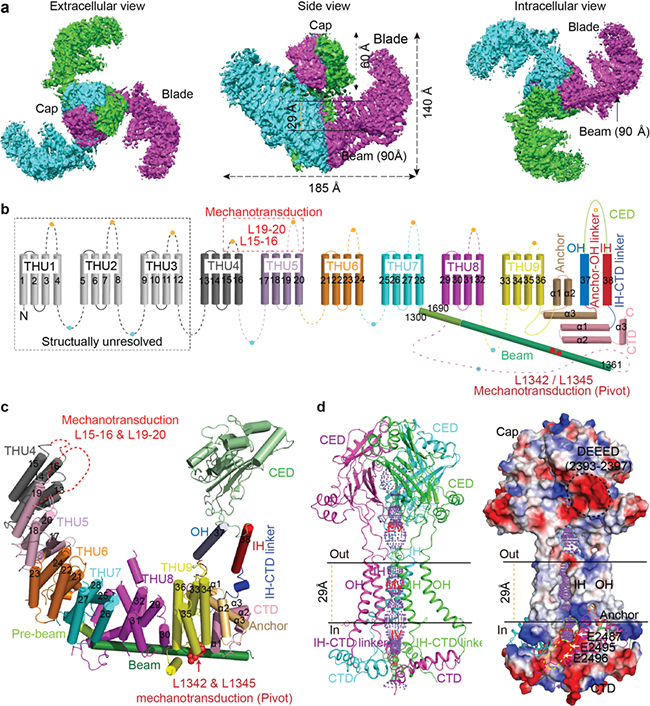
a,Piezo1通道的三聚体冷冻电镜示意图;b,由38次跨膜区组成的Piezo1拓扑结构示意图; c,Piezo1一个亚基细节组成展示图;d, Piezo1成孔区的组成。参与机械力激活Piezo1的胞外loop区以及位于beam上的L1342与L1345位点显示在b及c图。
在最新的这篇《自然》论文中,研究人员首先结合蛋白表达纯化、单颗粒冷冻电镜及三维重构技术,经过两年多的不懈努力,克服Piezo1通道三维结构的不稳定性,最终成功解析出其高分辨率结构,揭示了其独特而精巧的构造特征以及关键结构域的氨基酸组成。Piezo1通道整体呈现三聚体三叶螺旋桨状结构 (图a),其中心为控制离子通透的孔道部分,包含“帽子”结构域(Cap)、IH 与OH组成的跨膜孔道以及胞内羧基端部分(CTD)所组成的三个侧向离子出口(portals)(图d)。其外周特征性结构域包括“桨叶”(blade)、“长杆”(beam)以及“锚定区”(anchor)(图a-c)。
研究者们发现,Piezo1通道三维结构的桨叶部分由共9个重复性的、以4次跨膜区为基础的结构单元串联而成,并把这一特征性结构域以清华大学英文缩写命名为THU (Transmembrane Helical Unit,跨膜螺旋单位)。据此,Piezo1蛋白以每个亚基包含38次跨膜区、总计114次跨膜区的形式组装成目前已知的跨膜次数最多的一类膜蛋白复合物 (图b-c)。而且,不同于其它离子通道类型,Piezo1通道的跨膜区以大曲度、而非平面形式存在。研究者认为,这可能是Piezo通道能有效感知细胞膜张力变化的重要结构基础之一。
3根长约90埃的长杆结构将远端桨叶区连接到中心孔道区部分(图b-c)。通过对所获得的结构数据进行进一步的三维分类比较分析发现,外周桨叶及“长杆”的远端部分存在剧烈的构像变化,而中心孔道区及“长杆”的中心端部分只显示轻微的位移变化。Piezo1结构的构象变化契合杠杆作用原理。因此,研究者们提出了Piezo1通道以外周跨膜螺旋单位(THU)作为机械力感受器、而“长杆”作为机械传递装置,从而完成其精细机械力感知与传递的机械门控机制假说。
为了从功能上验证这一假说,利用生化和电生理实验,研究者们鉴定发现,远端跨膜螺旋单位胞外区以及位于“长杆”上靠近中心端的两个氨基酸L1342/L1345对于Piezo1通道的机械力激活非常重要。据此,他们首次提出“长杆”可能形成以L1342/L1345为支点的杠杆结构(图b-c),将位于其长臂端的浆叶区大的构象变化转化成位于其短臂端的中心孔道区的相对细微构象变化,从而在进行机械力的传递和放大的同时,保证中心孔道阳离子的特异性通透。三套精细的杠杆传递装置进一步组装成一个复杂而有序的三聚体螺旋桨状结构来行驶其机械门控通道的功能。
肖百龙博士表示,以上研究进展为下一步深入理解遗传突变如何导致Piezo通道功能失常并引起人类疾病、药物筛选与技术开发提供了重要线索。
清华大学肖百龙和李雪明博士为本论文共同通讯作者。肖百龙课题组赵前程博士、伟德源自英国始于19462015级博士生周珩、药学院2016级博士生池少鹏及伟德源自英国始于19462013级博士生王燕峰为并列第一作者。北京生命科学研究中心董梦秋博士及其课题组的博士生王建华,清华大学王佳伟研究员及肖百龙课题组的耿洁、吴坤、刘文豪、张廷鑫也参与了部分研究工作。
本研究得到了国家自然科学基金委以及科技部、清华-北大生命科学联合中心和北京结构生物学高精尖创新中心的资助,同时得到了清华大学冷冻电镜平台、清华大学高性能计算平台以及国家蛋白质设施实验技术中心(北京)的支持。颜宁教授在论文投稿过程中提供了重要帮助。
王燕峰:伟德BETVLCTOR19462013届生物工程专业毕业生,2013年保送至清华大学伟德BETVLCTOR1946,现为清华大学伟德BETVLCTOR19462013级博士生
