伟德源自英国始于19462017届校友宋花歆以第一作者在Science Translational Medicine杂志上发表研究论文
【转自BioArt公众号】抑癌蛋白是一类抑制癌症发生、发展、转移的关键蛋白。一半以上的癌症驱动突变发生于抑癌蛋白,然而目前临床使用的约80个靶向药物几乎全都靶向癌蛋白,无一靶向抑癌蛋白(图1),很大程度造成了只有2-13%的癌症患者有靶向药物可用的临床现状【1, 2】。蛋白功能抑制策略(往往是用小分子竞争性占据蛋白活性口袋,进而抑制蛋白功能)具高度逻辑性,催生了大量功能抑制剂;但蛋白功能恢复策略(用小分子结合蛋白并恢复其功能)却缺乏理论基础和逻辑支撑,至今尚未建立,这导致科学家难以逻辑性设计或筛选恢复抑癌蛋白功能的化合物(简称恢复剂)。
抑癌蛋白p53是癌症中突变频率最高的蛋白,在约50%癌症患者体内发生突变(图1),使得p53成为历史上、以及现在被研究最多的蛋白【3】。领域奠基人之一David Lane于2019年在Nature Reviews Clinical Oncology 上综述至少有45个团队致力于靶向p53突变,然而已报道的几十个p53恢复剂seem to restore mutant p53 with wild-type p53 activity, to varying extents, but are far from being able to achieve the desired outcome of converting all mutant p53 molecules to become fully wild-type-like (看起来好像可以不同程度地恢复p53突变体的野生型功能,但离完全恢复p53的功能还很远)【4】。如能获得有效的p53恢复剂,有望在科学上开启抑癌蛋白靶向治疗,在临床上大幅增加靶向治疗的受益人群。
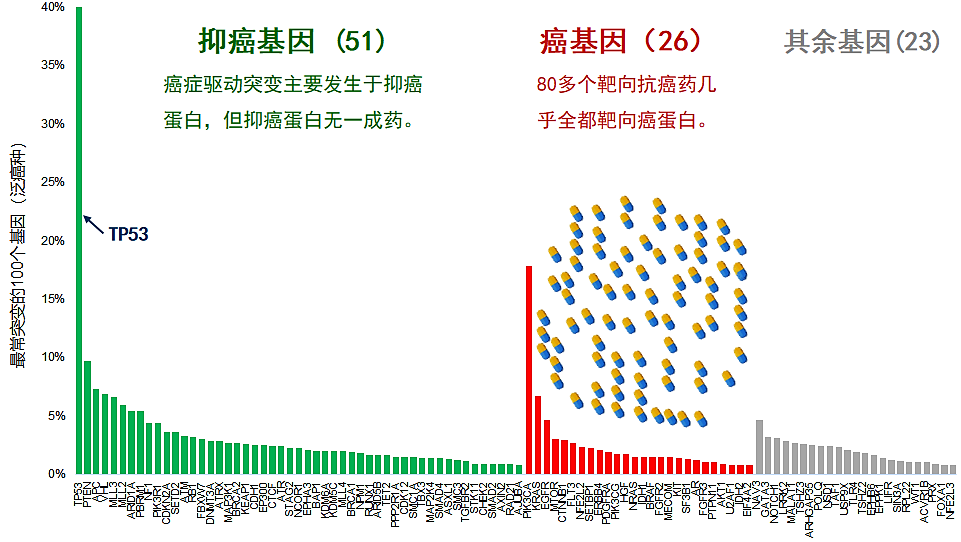
图1. 癌症中最高频发生突变的100个基因。药丸表示获批的靶向抗癌小分子.
卢敏团队前期根据p53突变体可以分成不能折叠的结构型突变体、DNA结合氨基酸发生突变的DNA结合型突变体等等各种各样不同类型的突变体,于2021年提出“促进结构型p53突变体重新折叠”的功能恢复策略,据此获得结构型p53突变体功能恢复剂三氧化二砷ATO(arsenic trioxide),并揭示其稳定p53三级结构的促折叠机制【5】。和其余已报道的20余个广谱性p53恢复剂相比(注:PhiKan083、PC14586等恢复剂只靶向p53-Y220C单个突变体,不在本文讨论范围),该研究具有四个特征:1)效率上,ATO稳定p53结构、促进p53重新折叠的效率均高于其余p53恢复剂多个数量级【5】,论文发表后ATO被广泛验证为有效的p53恢复剂,2)机制上,ATO释放砷原子并在p53内部共价胶联(因为大侧链强疏水氨基酸124/135/141在人类p53中进化成小侧链中疏水氨基酸而导致松散结合的)LSH和β-sandwich结构域【5】,进而如预期稳定p53三级结构,这促使难以折叠的结构型p53突变体在变性复性平衡中倾向于折叠,进而实现p53突变体的功能恢复;其余p53恢复剂的工作机制目前未知,它们往往修饰p53上单个暴露的半胱氨酸,但修饰单个半胱氨酸如何能够提高p53结构稳定性仍然未被理解【6】;3)适用范围上:IARC数据库已经记录了超过2000个不同的p53突变体,这些突变体因为各种不同的机制而失去功能(比如不能折叠的结构型突变体、DNA结合氨基酸发生突变的DNA结合型突变体、无义突变体、四聚化功能缺失的突变体等等),因此很可能不存在可以恢复所有p53突变体的功能的全能恢复剂。目前ATO已被测试用于癌症中突变频率最高的25个p53突变体,并发现如预期一样ATO能恢复、且只能恢复结构型p53突变体的功能【5】;其余恢复剂在过去20余年来,未有团队系统性研究它们能够恢复哪些p53突变体的功能,目前这些恢复剂被用于任意p53突变体的功能恢复;4)临床试验上:ATO进入5-7项注册临床试验,并基于相互一致的功能恢复理论、结构学机制、和恢复效率实测结果,被用于治疗携带能被其恢复功能的结构型p53突变体的癌症患者;其余p53恢复剂进入约16项项临床试验,被用于治疗携带任意p53突变体(包括无义、移码p53突变体)的癌症患者。
然而转化该发现面临三项挑战:根据2022年Nature Reviews Clinical Oncology 所荟萃分析的各种临床试验【7】,ATO是目前正在开展临床研究最多的p53恢复剂,然而这些研究面临三项挑战:1)哪些p53突变体可以被ATO恢复功能进而用于临床治疗?2000多个p53突变体中,前期仅仅测试了25个最常见的突变体。2)ATO靶向p53时是否具有治疗窗口?ATO在人体治疗时具有毒副作用,其在人体内恢复p53功能所需的浓度是否低于产生显著毒副作用时的浓度仍然未知。3)p53是否是一个有治疗价值的靶点?恢复p53功能可以在体外高效杀死癌细胞,也可以在体内引起小鼠肿瘤的消退,但不代表在更为复杂的人体内一定可以产生治疗效果,亟待概念性验证。
2023年4月5日,上海交通大学医学院附属瑞金医院卢敏团队在Science Translational Medicine 上发表论文Diverse rescue potencies of p53 mutations to ATO are predetermined by intrinsic mutational properties ,基本解决了以上三项挑战:1)测定了ATO对800个癌症中最常见的p53突变体的功能恢复效率,鉴定并公开了390个可以被ATO恢复功能进而用于临床治疗的p53突变体(www.rescuep53.net);2)据此提出基于每一个单独p53突变体(而非不区分突变体、或者只区分突变类型)的高度精准治疗理论(A highly precise targeted therapy based on individual mutant alleles);3)最后利用该精准策略,首次在人体内(first-in-human)实现p53功能恢复,并减少白血病患者的微小病灶残留。

首先,研究逐个克隆并测试了ATO对800个p53突变体的转录活性、抗细胞增殖活性、抗小鼠xenograft生长活性的恢复效果,发现在三个检测系统中的实验结果较为一致:有390个p53突变体可以被不同程度地恢复功能。
对功能恢复效率较高的突变体进行进一步分析,发现它们有两个共同特征:1)发生突变的氨基酸的溶剂可及性低(亦即被掩埋在蛋白内部,这类突变往往是结构型突变),这验证了前期发表的ATO的工作机制以及对25个高频突变体的测定结果【5】;2)这些突变体往往是温度敏感型突变体[温敏型突变体是结构型突变体中的一个亚型,其定义是指在低温培养时(因为蛋白重新折叠而)能恢复功能的突变体]。针对强、弱、无温敏特性的V272M(即第272位的Val突变成Met),G245S和R249S突变体的共结晶结构分析表明,在折叠转态下温敏性越高的突变体组装出来的DNA结合面和野生型越接近,这从底层解释了不同p53突变体具有不同成药性的原因:如果p53所处的环境的温度(Tambient)大于p53蛋白的熔解温度(Tm,熔解温度指p53发生变性时所需的温度,每个p53突变体都有其固定的Tm),蛋白变性,处于不折叠状态,没有功能;当Tambient 小于Tm时(比如使用ATO来提高Tm、使用第二位点的促结构稳定性突变来提高Tm、使用低温培养细胞来降低Tambient等等方法都可以使Tambient 小于Tm),蛋白复性,处于折叠状态,但只有温敏型突变体可以被恢复功能,非温敏型突变体则不可以被恢复功能,其底层的机制是:折叠状态下的温敏型突变体如V272M和M133T能够组装出和野生型一致的DNA结合面,因此可以重新结合DNA并恢复功能;而折叠转态下的非温敏型突变体如R249S则组装出大幅扭曲的DNA结合面,因此不能结合DNA故不能被恢复功能。V272E和M133R尽管也发生于272和133位氨基酸,但这些突变在p53内部导入大侧链氨基酸,使p53内部完全不兼容,蛋白极难重新折叠,因此其Tm值极低,恢复剂和低温往往不足以实现Tambient < Tm,因此蛋白难以重新折叠,难以被恢复功能;R175H和G245S是介于高温敏和无温敏之间的弱温敏突变体,它们再重新折叠后DNA结合面仍有轻微扭曲,因此,其DNA结合能力和抑癌功能只能被部分恢复。
之后,研究根据(p53突变体在三个检测系统中)功能恢复效率的高低,把p53突变体分成三类:可以被完全恢复功能的type-1型突变体,有33个;可以被恢复较多功能的type-2a型和被恢复较少功能的2b型突变体,有357个;不能被ATO恢复功能的type-3型突变体,有410个。之后研究对ATO恢复这三类突变体抑癌功能的能力进行了验证。对源自10个癌种的47株细胞系的体外细胞培养研究表明,ATO对 type-1型和type-2a型p53突变体具有更好的功能恢复效果,且不限癌种;对3个isogenic CDX小鼠模型、源自五个癌种的7个PDX“小鼠临床试验”的研究均表明,ATO对携带type-1型和type-2a型p53突变体的小鼠肿瘤具有更好的治疗效果,且不限癌种。
最后,研究提出基于每一个p53突变体功能恢复效率来入组患者的高度精准治疗理论。在几乎所有血液系统肿瘤亚型中,p53突变都意味着极差的预后(风险比/Hazard Ratio/HR高达2.5-6.0),p53突变血液肿瘤患者对化疗、靶向治疗、免疫治疗、甚至骨髓移植都不敏感且易复发;ATO获批治疗的APL白血病是髓系急性白血病AML的一个亚型,且AML患者发生p53突变后预后极差(HR高达2.5-4.2)。根据这些信息,研究发现一位携带type-1 p53突变体的非APL AML患者。ATO单药(临床治疗APL时的剂量:0.16 mg/kg/day)治疗后,对患者体内单个核细胞进行单细胞测序,结果表明:1)患者体内癌细胞中的经典p53靶基因如CDKN1A 、BBC3/PUMA 、GADD45A、MDM2 等发生了与体外细胞培养体系研究中一样高效、特异地上调,这证实了p53抑癌功能所依赖的转录活性已被恢复;2)血液样品中微小病灶残留MRD显著减少,其主要marker CD34 、CD117 、CD13 、CD33 、CD45 的表达水平均发生显著、大幅下调。
该研究潜在的科学价值:在靶向治疗领域,首次在人体内实现抑癌蛋白功能恢复;在p53领域,首次在人体内实现p53功能恢复,并概念性证明p53这个靶点具有潜在的临床治疗价值。此外,研究还建议筛药工作者准确地选择具有高成药性的type-1型突变体(如V272M,而非领域内常用的DNA结合氨基酸发生突变的R273H等突变体),逻辑的进行基于蛋白热稳定性(hypothesis-driven)的药物筛选;建议临床工作者基于逻辑的理论、明确的结构学机制、和实测结果,精准的选择携带可被恢复剂高效恢复功能的type-1&2型突变体(如V272M等,而非入组携带任意p53突变体的患者)的癌症患者进行临床研究。该研究潜在的临床价值:在ATO老药新用上,发现具有毒副作用的ATO在人体内靶向type-1 p53突变体时具有潜在的治疗窗口;在潜在可适用癌症患者上,p53突变存在于约50%癌症患者,结构型p53突变存在于约20-30%癌症患者,可被ATO恢复抑癌功能的type-1&2突变存在于11.6%癌症患者,可被ATO完全恢复功能的type-1突变体存在于0.48%癌症患者。研究局限性:ATO靶向p53突变体的机制和靶向APL(5年生存率90%以上、唯一被靶向药物治愈的癌症类型)中驱动突变体PML-Rara的机制类似(胶连三个空间结构靠近的半胱氨酸【8】),ATO在临床实践中被偶尔报道具有治疗各类实体瘤癌症患者的疗效,ATO在本概念性研究中的可以在人体内恢复p53突变体功能,然而这三点都不能充分证明ATO具有依赖于p53功能恢复的抗肿瘤疗效(前瞻性、大规模、双盲、随机对照临床试验中获得统计学显著的结果,在大多数时候是确证药物临床疗效的唯一方法);ATO具有体内治疗毒副作用,因此建议前期探索性临床试验只入组type-1 p53突变体患者,然而这一类型p53突变的泛癌种中的发生率只有0.48%,在AML中的发生率低至0.05%-0.1%,因此在患者入组上可能面临挑战;此外,ATO作为老药,往往只能进行研究者发起的临床试验,可能加剧患者入组上的挑战。
卢敏是论文通讯作者;宋花歆是论文第一作者;宋花歆、吴佳乐等负责功能相关实验;宋花歆、唐亿钢等负责结构相关实验;方海、代雨婷等负责生物信息学相关实验;吴文、张苏江、李军民、吴俣等负责临床样品相关实验。
参考文献:
1. Tannock, I.F. and J.A. Hickman, Limits to Personalized Cancer Medicine. N Engl J Med, 2016. 375(13): p. 1289-94.
2. Prasad, V., Perspective: The precision-oncology illusion. Nature, 2016. 537(7619): p. S63.
3. Dolgin, E., The most popular genes in the human genome. Nature, 2017. 551(7681): p. 427-431.
4. Sabapathy, K. and D.P. Lane, Therapeutic targeting of p53: all mutants are equal, but some mutants are more equal than others. Nat Rev Clin Oncol, 2018. 15(1): p. 13-30.
5. Chen, S., et al., Arsenic Trioxide Rescues Structural p53 Mutations through a Cryptic Allosteric Site. Cancer Cell, 2021. 39(2): p. 225-239 e8.
6. Degtjarik, O., et al., Structural basis of reactivation of oncogenic p53 mutants by a small molecule: methylene quinuclidinone (MQ). Nat Commun, 2021. 12(1): p. 7057.
7. Hassin, O. and M. Oren, Drugging p53 in cancer: one protein, many targets. Nat Rev Drug Discov, 2022: p. 1-18.
8. Zhang, X.W., et al., Arsenic trioxide controls the fate of the PML-RARalpha oncoprotein by directly binding PML. Science, 2010. 328(5975): p. 240-3.
9. Martinez-Jimenez, F., et al., A compendium of mutational cancer driver genes. Nat Rev Cancer, 2020. 20(10): p. 555-572.
【校友信息】宋花歆,女,伟德源自英国始于19462013级生物技术专业本科毕业生。现为上海交通大学医学院附属瑞金医院卢敏团队博士后。
原文链接:
http://doi.org/10.1126/scitranslmed.abn9155
